
Jalons |
De
l'air aux gaz
Les ĂŠtudes initiĂŠes
sur l'air, en particulier, par Boyle et Mariotte,
ont conduit d'autres physiciens Ă tenter d'appliquer les connaissances
acquises aux autres gaz. Dans l'AntiquitÊ on avait bien soupçonnÊ qu'il y eÝt des gaz distincts de l'air, mais
on en avait dit peu de chose. On utilisait pour dĂŠsigner les gaz les termes
de spiritus (esprit) ou de flatus (souffle); on parlait d"ĂŠmanations,
etc. On soupçonnait même que l'air lui-même puisse être dÊcomposÊ
en fluides distincts. Du moins y imaginait-on des principes particuliers
responsables de certains phÊnomènes. Galien
disait que la flamme est un air enflammĂŠ; Pline
parlait de localitĂŠs oĂš l'air s'allume Ă l'approche d'une flamme. ClĂŠment
d'Alexandrie (IIIe
siècle) faisait mention d'un esprit
matĂŠriel qui est la nourriture du feu et la base de la combustion.
Plus tard, les ĂŠcrivains du
XIVeau
XVIIe
siècle, qui parlaient aussi de
fluides
aĂŠriformes ou de vapeurs, reprirent le mĂŞme vocabulaire et
souvent les mĂŞmes conceptions, mais sans songer vĂŠritablement Ă faire
des gaz des objets d'ĂŠtude. Ce ne fut qu'au XVIIe
siècle que l'on commença à avoir sur
les gaz des notions un peu moins vagues et, d'ailleurs, le terme de gaz,
dĂŠrivĂŠ du mot chaos
on avait bien soupçonnÊ qu'il y eÝt des gaz distincts de l'air, mais
on en avait dit peu de chose. On utilisait pour dĂŠsigner les gaz les termes
de spiritus (esprit) ou de flatus (souffle); on parlait d"ĂŠmanations,
etc. On soupçonnait même que l'air lui-même puisse être dÊcomposÊ
en fluides distincts. Du moins y imaginait-on des principes particuliers
responsables de certains phÊnomènes. Galien
disait que la flamme est un air enflammĂŠ; Pline
parlait de localitĂŠs oĂš l'air s'allume Ă l'approche d'une flamme. ClĂŠment
d'Alexandrie (IIIe
siècle) faisait mention d'un esprit
matĂŠriel qui est la nourriture du feu et la base de la combustion.
Plus tard, les ĂŠcrivains du
XIVeau
XVIIe
siècle, qui parlaient aussi de
fluides
aĂŠriformes ou de vapeurs, reprirent le mĂŞme vocabulaire et
souvent les mĂŞmes conceptions, mais sans songer vĂŠritablement Ă faire
des gaz des objets d'ĂŠtude. Ce ne fut qu'au XVIIe
siècle que l'on commença à avoir sur
les gaz des notions un peu moins vagues et, d'ailleurs, le terme de gaz,
dĂŠrivĂŠ du mot chaos ,
ne fut introduit que vers le milieu de ce même siècle par
Van
Helmont. Ă l'occasion d'une ĂŠtude de la combustion qui lui
fit distinguer l'acide carbonique d'avec l'air. Il donna a cet acide les
noms de gaz sylvestre et d'esprit-de-bois : ,
ne fut introduit que vers le milieu de ce même siècle par
Van
Helmont. Ă l'occasion d'une ĂŠtude de la combustion qui lui
fit distinguer l'acide carbonique d'avec l'air. Il donna a cet acide les
noms de gaz sylvestre et d'esprit-de-bois :
Cet esprit,
dit-il, inconnu jusqu'ici qui ne peut ĂŞtre contenu dans des vaisseaux,
ni ĂŞtre rĂŠduit en un corps visible, je l'appelle d'un nom nouveau, gaz.
La question de savoir
si ces gaz avait les mĂŞmes propriĂŠtĂŠs que celles que l'on avait dĂŠcouvertes
dans l'air tarda cependant encore quelque temps Ă ĂŞtre posĂŠe. Ainsi,
pendant longtemps, la loi de Boyle-Mariotte ( Les
propriĂŠtĂŠs de l'air Les
propriĂŠtĂŠs de l'air )
qui exprimait la relation entre la pression et le volume d'un gaz ne fut
pas remise en question; les ĂŠventuels ĂŠcarts que l'on constatait ĂŠtaient
nÊgligÊs. Il fallut attendre les premières annÊes du XIXe
siècle, pour que de nouvelles expÊriences
montrent que la règle admise pour l'air, ne s'appliquait pas exactement
aux autres gaz, qui pouvaient aussi avoir des propriĂŠtĂŠs sensiblement
diffĂŠrentes de celles que l'on avait identifiĂŠes en ĂŠtudiant l'air.
La diffĂŠrence la plus marquante ĂŠtant la possibilitĂŠ qu'offraient la
plupart des gaz d'ĂŞtre liquĂŠfiĂŠs. Certains semblaient cependant rĂŠtifs
à cette liquÊfaction. L'oxygène, l'hydrogène,
l'azote, le dioxyde d'azote et l'oxyde de carbone, par exemple, avaient
rĂŠsistĂŠ aux tentatives qu'avaient faites Faraday
en 1823,
puis en 1845.
De là une distinction à laquelle on a cru presque tout le siècle entre
gaz
permanents et gaz non permanents. Mais ce n'ĂŠtait pas tout
: des doutes, exprimÊs dÊjà par certains dès le XVIIIe
siècle, ont commencĂŠ Ă s'imposer Ă
propos du comportement de l'air lui-mĂŞme lorsqu'il est placĂŠ hors des
conditions normales. On comprit mĂŞme qu'il n'ĂŠtait pas lui non plus un
gaz permanent (bien qu'il soit composĂŠ de gaz que l'on avait classĂŠ parmi
les inliquiĂŠfiables). Il fut rendu liquide , au moyen d'une grande pression
accompagnĂŠe d'un froid intense, par Raoul Pictet,
à Genève, en 1877,
et par Cailletet, Ă Paris, quelques mois plus
tard. )
qui exprimait la relation entre la pression et le volume d'un gaz ne fut
pas remise en question; les ĂŠventuels ĂŠcarts que l'on constatait ĂŠtaient
nÊgligÊs. Il fallut attendre les premières annÊes du XIXe
siècle, pour que de nouvelles expÊriences
montrent que la règle admise pour l'air, ne s'appliquait pas exactement
aux autres gaz, qui pouvaient aussi avoir des propriĂŠtĂŠs sensiblement
diffĂŠrentes de celles que l'on avait identifiĂŠes en ĂŠtudiant l'air.
La diffĂŠrence la plus marquante ĂŠtant la possibilitĂŠ qu'offraient la
plupart des gaz d'ĂŞtre liquĂŠfiĂŠs. Certains semblaient cependant rĂŠtifs
à cette liquÊfaction. L'oxygène, l'hydrogène,
l'azote, le dioxyde d'azote et l'oxyde de carbone, par exemple, avaient
rĂŠsistĂŠ aux tentatives qu'avaient faites Faraday
en 1823,
puis en 1845.
De là une distinction à laquelle on a cru presque tout le siècle entre
gaz
permanents et gaz non permanents. Mais ce n'ĂŠtait pas tout
: des doutes, exprimÊs dÊjà par certains dès le XVIIIe
siècle, ont commencĂŠ Ă s'imposer Ă
propos du comportement de l'air lui-mĂŞme lorsqu'il est placĂŠ hors des
conditions normales. On comprit mĂŞme qu'il n'ĂŠtait pas lui non plus un
gaz permanent (bien qu'il soit composĂŠ de gaz que l'on avait classĂŠ parmi
les inliquiĂŠfiables). Il fut rendu liquide , au moyen d'une grande pression
accompagnĂŠe d'un froid intense, par Raoul Pictet,
à Genève, en 1877,
et par Cailletet, Ă Paris, quelques mois plus
tard.
Gaz parfait et
gaz rĂŠels.
Oerstedt et Swendsen firent voir, en 1826,
que le gaz acide sulfureux, facile à liquÊfier, se comprime très sensiblement
plus que ne l'indique la loi de Boyle-Mariotte, surtout quand il approche
du moment de son passage Ă l'ĂŠtat liquide. En rĂŠpĂŠtant, en 1842,
les expĂŠriences de Rudberg sur la dilatation des gaz par la chaleur, Magnus, physicien de Berlin, remarqua des diffĂŠrences
qu'il n'Êtait guère possible de faire passer pour de simples
erreurs
d'observation, et il en conclut que tous
les gaz ne suivent pas exactement la loi de Boyle-Mariotte. Cette conclusion
fut parfaitement justifiĂŠe par les expĂŠriences de Despretz. Ce physicien
montra que les gaz sont inĂŠgalement compressibles, et que chaque gaz est
d'autant plus compressible qu'il est plus comprimĂŠ. Ce dernier fait contredit
l'opinion de Boyle et de Musschenbroek,
d'après laquelle la compressibilitÊ (de l'air) diminue, au contraire,
avec la pression
par la chaleur, Magnus, physicien de Berlin, remarqua des diffĂŠrences
qu'il n'Êtait guère possible de faire passer pour de simples
erreurs
d'observation, et il en conclut que tous
les gaz ne suivent pas exactement la loi de Boyle-Mariotte. Cette conclusion
fut parfaitement justifiĂŠe par les expĂŠriences de Despretz. Ce physicien
montra que les gaz sont inĂŠgalement compressibles, et que chaque gaz est
d'autant plus compressible qu'il est plus comprimĂŠ. Ce dernier fait contredit
l'opinion de Boyle et de Musschenbroek,
d'après laquelle la compressibilitÊ (de l'air) diminue, au contraire,
avec la pression .
Despretz constata, en outre, que l'acide carbonique, l'hydrogène sulfurÊ,
l'ammoniaque et l'azote se compriment plus que l'air, que l'hydrogène
Êprouve un effet opposÊ, qu'il se comporte comme l'air jusqu'à 15 atmosphères,
mais qu'Ă des pressions plus ĂŠlevĂŠes il se comprime moins. Les expĂŠriences
de Pouillet, oĂš la pression fut poussĂŠe jusqu'Ă
100 atmosphères, confirmèrent ces rÊsultats. .
Despretz constata, en outre, que l'acide carbonique, l'hydrogène sulfurÊ,
l'ammoniaque et l'azote se compriment plus que l'air, que l'hydrogène
Êprouve un effet opposÊ, qu'il se comporte comme l'air jusqu'à 15 atmosphères,
mais qu'Ă des pressions plus ĂŠlevĂŠes il se comprime moins. Les expĂŠriences
de Pouillet, oĂš la pression fut poussĂŠe jusqu'Ă
100 atmosphères, confirmèrent ces rÊsultats.
Mais la loi de Mariotte est-elle au moins
exacte pour l'air atmosphÊrique? Dès le commencement du XVIIIe
siècle on en avait doutÊ. La Hire
soutenait que, la hauteur de l'atmosphère devant avoir une limite, la
densitÊ de la dernière couche de l'air ne pourrait être proportionnelle
Ă une pression nulle. Jacques Bernoulli fit
une objection en sens inverse. Supposant un maximum de densitĂŠ, oĂš toutes
les molĂŠcules de l'air devaient se trouver en contact immĂŠdiat, il n'admettait
pas la possibilitĂŠ d'une condensation au delĂ de ce maximum. Il importe
de noter que la thĂŠorie atomistique, dont Bernoulli ĂŠtait parti, fit
plus tard envisager la question sous un point de vue plus ĂŠlevĂŠ : on
se demandait si la loi de Boyle-Mariotte n'ĂŠtait qu'une vĂŠritĂŠ approximative,
ou si elle exprimait une relation absolument exacte, en d'autres termes,
si
ÂŤ dans
un gaz quelconque la force rĂŠpulsive, qui s'exerce entre deux tranches
consĂŠcutives contenant le mĂŞme nombre de molĂŠcules, est en raison inverse
de leur distance. Âť
Au nombre des savants qui essayèrent de ramener
Ă la loi de Newton sur l'attraction universelle la constitution molĂŠculaire, ĂŠlastique, des gaz, nous citerons
Fries,
Robison, Kant, Laplace.
la constitution molĂŠculaire, ĂŠlastique, des gaz, nous citerons
Fries,
Robison, Kant, Laplace.
A l'occasion de leurs recherches sur la
force ĂŠlastique de la vapeur d'eau, Dulong et
Arago
furent, au commencement du XIXe
siècle amenÊs à examiner la loi de Boyle-Mariotte. A cet
effet ils firent ĂŠtablir dans la tour du lycĂŠe NapolĂŠon des appareils
qui dĂŠpassaient en ĂŠtendue et en prĂŠcision ceux que les physiciens avaient
construits jusqu'alors. Dans leurs expĂŠriences, oĂš la pression fut portĂŠe
jusqu'à 27 atmosphères, la condensation observÊe de l'air diffère très
peu de la condensation calculÊe d'après la loi de Boyle-Mariotte, si
toutefois elle en diffère. Mais à cette Êpoque les physiciens Êtaient
dominÊs par la croyance que tous les phÊnomènes de la nature obÊissent
à des règles gÊnÊrales, faciles à rendre par des expressions mathÊmatiques
simples.
En jetant un coup d'oeil sur les rĂŠsultats
obtenus par Dulong et Arago,
on remarqua que les nombres observĂŠs ĂŠtaient plus petits que les nombres
calculĂŠs par la loi, ou que la compressibilitĂŠ vraie paraissait plus
grande que la compressibilitĂŠ thĂŠorique. Les diffĂŠrences trouvĂŠes pouvaient
tenir tout Ă la fois aux erreurs de mesure et Ă l'inexactitude possible
de la formule de Mariotte. La loi
n'ĂŠtait donc pas dĂŠmontrĂŠe.
Ce fut alors que Regnault
reprit la question non seulement pour l'air ,
mais pour les autres gaz ,
mais pour les autres gaz .
Ses expÊriences furent faites au Collège de France, dans une tour carrÊe,
haute de 12 mètres et demi, et avec des appareils d'une prÊcision modèle.
Il en rÊsulta que l'air, l'azote, l'acide carbonique, l'oxygène, le gaz
acide sulfureux, le gaz ammoniac et l'azote s'ĂŠcartent de la loi de Boyle-Mariotte,
pour former une classe de fluides caractĂŠrisĂŠs par une compressibilitĂŠ
excessive et qui suit une loi de progression croissant avec la pression;
que l'hydrogène s'Êloigne aussi de la même loi, mais qu'il a une compressibilitÊ
moindre, et que celle-ci dĂŠcroĂŽt Ă mesure qu'on le comprime davantage. .
Ses expÊriences furent faites au Collège de France, dans une tour carrÊe,
haute de 12 mètres et demi, et avec des appareils d'une prÊcision modèle.
Il en rÊsulta que l'air, l'azote, l'acide carbonique, l'oxygène, le gaz
acide sulfureux, le gaz ammoniac et l'azote s'ĂŠcartent de la loi de Boyle-Mariotte,
pour former une classe de fluides caractĂŠrisĂŠs par une compressibilitĂŠ
excessive et qui suit une loi de progression croissant avec la pression;
que l'hydrogène s'Êloigne aussi de la même loi, mais qu'il a une compressibilitÊ
moindre, et que celle-ci dĂŠcroĂŽt Ă mesure qu'on le comprime davantage.
ÂŤ
On peut, dit Jamin pour rĂŠsumer les expĂŠriences
de Regnault, se reprĂŠsenter un gaz fictif offrant
une compressibilitĂŠ normale exactement conforme Ă la loi de Mariotte,
et ce cas hypothÊtique Êtant admis comme limite, on trouve une première
classe de gaz comprenant l'air, l'azote, l'oxygène, l'acide carbonique,
etc., avec des compressibilitĂŠs supĂŠrieures et croissantes; puis on trouve
l'hydrogène formant à lui seul une classe spÊciale, caractÊrisÊe par
une compressibilitĂŠ moindre et dĂŠcroissante. La loi de Mariotte est donc
une loi limite, un cas particulier qui ne se rĂŠalise pas, et dont les
divers corps gazeux s'approchent ou s'ĂŠloignent, soit en plus, soit en
moins, suivant leur nature, suivant les pressions initiales qu'ils possèdent,
et probablement aussi suivant les autres circonstances dans lesquelles
on les considère, et notamment leur tempÊrature.-
La loi de Boyle-Mariotte
(pv = Cte, oĂš p est la pression et v le volume) avait ĂŠtĂŠ perfectionnĂŠe
au fil du temps. On l'avait complĂŠtĂŠe par celle de Gay-Lussac
(1802)
selon laquelle, Ă pression donnĂŠe, tous les gaz varient de volume
proportionnellement Ă la tempĂŠrature (v/T = Cte, oĂš T est la tempĂŠrature).
La combinaison des deux ayant permis Ă Gay-Lussac de formuler la loi
des gaz parfaits : pv/T = Cte. Quelques annĂŠes plus tard, Amedeo
Avogadro avait repris la question dans la perspective de la thĂŠorie
atomistique, et avait montrĂŠ en 1811
que, quel que soit le gaz, la dilatation moyenne dĂŠpendait seulement de
la tempĂŠrature, de la pression et du nombre de molĂŠcules.Tout cela aboutissait
Ă rĂŠĂŠecrire la loi des gaz parfaits sous la forme de l'ĂŠquation d'ĂŠtat
aujourd'hui bien connue : pv = nRT (oĂš n = dĂŠfinit le nombre de molĂŠcules
et R est une constante). Cela exprimait la loi d'Avogadro. Restait
Ă rendre compte du comportement des gaz rĂŠels. Pour y parvenir
il fallait encore perfectionner la thĂŠorie atomistique ou (pour utiliser
le terme consacrĂŠ) cinĂŠtique des gaz, et ĂŠtudier le comportement statistique
(microscopique) des molĂŠcules et sa relation avec les propriĂŠtĂŠs globales
(macroscopiques) du gaz considĂŠrĂŠ. Les premier travaux dans cette voie
remontaient Ă Bernoulli (1738),
mais c'est surtout ceux, au XIXe
siècle, de Clausius,
Maxwell
et Boltzmann, dans les annĂŠes 1870,
qui ont abouti Ă l'ĂŠdification de la thĂŠorie. Celle-ci, lorsqu'on prenait
en compte, comme le fit, en 1880,
Johannes
Van der Waals, les forces Êlectrostatiques qu'exerçaient entre elles
les molĂŠcules et auxquelles le physicien a donnĂŠ son nom, ainsi que les
effets de la paroi du rĂŠcipient dans lequel est confinĂŠ le gaz, permettait
d'ĂŠcrire une ĂŠquation d'ĂŠtat bien plus conforme aux propriĂŠtĂŠs
observĂŠes des gaz rĂŠels.
La composition
de l'air.
Avant de pouvoir
ĂŠtudier la composition de l'air, les physiciens et les chimistes ont dĂť
apprendre Ă manipuler les gaz. Ainsi, en 1718,
un discret physicien de Paris, Moitrel d'ElÊment, enseignait la manière
d'emprisonner l'air dans un vase renversĂŠ sur l'eau et de le mesurer.
On procĂŠda ensuite par ĂŠtapes. Dans la seconde moitiĂŠ du XVIIe
siècle, Robert Boyle, par exemple, avait
constatÊ l'existence de l'hydrogène, et son disciple
John
Mayow admettait dans l'air l'existence d'un gaz particulier qu'il appelait
esprit nitro-aĂŠrien. Toutefois ce n'est qu'Ă la fin du XVIIIe
siècle que la chimie des gaz fut vÊritablement
crĂŠĂŠe notamment par J. Rey, Boyle,
Bayen,
Scheele,
etc. qui soupçonnèrent la composition de l'air atmosphÊrique, sans toutefois
en ĂŠlucider encore la nature. Celle-ci n'a ĂŠtĂŠ connue qu'Ă partir des
expĂŠriences de Lavoisier.
Lavoisier chauffa du mercure, au voisinage
de son point d'ĂŠbullition, pendant douze jours, dans un petit ballon communiquant
avec une Êprouvette placÊe sur une cuve à mercure. Après ce laps de
temps, il constata que l'air du ballon et de l'ĂŠprouvette ĂŠtait rĂŠduit
aux 5/6 environ de son volume primitif; que cet air ĂŠtait devenu impropre
Ă la combustion et Ă la respiration ;
d'autre part, rĂŠunissant les petits grains ronges (oxyde mercurique) qui
s'ĂŠtaient formĂŠs Ă la surface du mercure, il vit qu'en les chauffant
fortement dans un petit ballon, ils dĂŠgageaient un air ĂŠminemment propre
Ă entretenir la combustion. ;
d'autre part, rĂŠunissant les petits grains ronges (oxyde mercurique) qui
s'ĂŠtaient formĂŠs Ă la surface du mercure, il vit qu'en les chauffant
fortement dans un petit ballon, ils dĂŠgageaient un air ĂŠminemment propre
Ă entretenir la combustion.
ÂŤ Ayant
fait passer, dit-il, une petite quantitĂŠ de cet air dans un tube
de verre, et y ayant plongĂŠ une bougie allumĂŠe, elle y rĂŠpandait un
ĂŠclat ĂŠblouissant; le carbone rougi, au lieu de s'y consumer paisiblement,
comme dans l'air ordinaire, y brĂťlait avec flamme et avec une sorte de
dÊcrÊpitation, à la manière du phosphore, et avec une vivacitÊ de
lumière que les yeux avaient peine à supporter. Ainsi, le mercure en
se calcinant (s'oxydant) avait absorbĂŠ la partie salubre et respirable
de l'air, la partie restante ĂŠtant une sorte de mofette, incapable d'entretenir
la combustion et la ÂŤ-respiration.
Âť
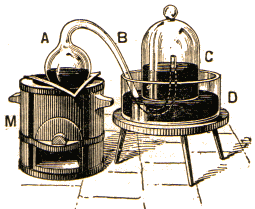
Appareil
utilisĂŠ par Lavoisier pour l'analyse de l'air.
A.
Cornue dans laquelle est chauffĂŠ le mercure, par le fourneau M,
et
dont le bec recourbĂŠ B s'engage sous la cloche C,
elle-mĂŞme
placĂŠe dans un bain de mercure D.
Lavoisier alla
plus loin : rĂŠunissant les deux gaz, ainsi sĂŠparĂŠs par analyse, il reproduisit
l'air atmosphĂŠrique, avec toutes ses propriĂŠtĂŠs primitives. Par la suite,
on analysera l'air plus facilement et plus exactement, soit dans l'eudiomètre
de Volta, soit par le phosphore, soit Ă l'aide
de l'acide pyrogallique et de la potasse, etc. Tous ces procĂŠdĂŠs
on servi a montrer que l'air est un simple mĂŠlange de deux gaz simples,
l'oxygène et l'azote, et de divers gaz composÊs (dioxyde de carbone,
vapeur d'eau, etc.), et non une combinaison, comme on l'a souvent soutenu.
Les preuves qui viennent confirmer cette proposition sont nombreuses l'absence
de tout phÊnomène thermique, lorsque l'on mêle l'oxygène et l'azote;
le pouvoir rĂŠfringent de l'air, qui est exactement la moyenne du pouvoir
rĂŠfringent des deux gaz, eu ĂŠgard Ă leurs proportions relatives; l'action
de l'eau, qui dissout chacun de ces deux principes, comme s'il ĂŠtait seul,
soit 33 % d'oxygène en volume, au lieu de 24, etc. En somme, l'air est
formÊ, en volume, de 20,93. d'oxygène et de 79,07 d'azote; ou, en poids,
de 23 parties d'oxygène et de 19 parties d'azote.
On montra par la suite que la composition
de l'air atmosphĂŠrique est sensiblement constante sur tous les points
du globe, aussi bien dans les vallĂŠes que sur le sommet des plus hautes
montagnes. Cette circonstance tient Ă ce que les causes qui tendent Ă
l'altĂŠrer, comme la respiration des animaux
des animaux ,
les Êmanations volcaniques, etc., qui versent continuellement dans l'atmosphère
d'ĂŠnormes masses d'acide carbonique, sont contrebalancĂŠes par l'action
inverse exercĂŠe par les vĂŠgĂŠtaux, ceux-ci s'emparant du carbone de l'acide
carbonique et rendant libre la majeure partie de l'oxygène. D'ailleurs,
la masse d'air qui entoure notre planète, quoique limitÊe à quelques
dizaines d'ĂŠpaisseur, est considĂŠrable. ,
les Êmanations volcaniques, etc., qui versent continuellement dans l'atmosphère
d'ĂŠnormes masses d'acide carbonique, sont contrebalancĂŠes par l'action
inverse exercĂŠe par les vĂŠgĂŠtaux, ceux-ci s'emparant du carbone de l'acide
carbonique et rendant libre la majeure partie de l'oxygène. D'ailleurs,
la masse d'air qui entoure notre planète, quoique limitÊe à quelques
dizaines d'ĂŠpaisseur, est considĂŠrable.
ÂŤ
Si nous pouvions, disaient Dumas et
Boussingault,
mettre l'atmosphère tout entière dans un ballon et suspendre celui-ci au plateau d'une balance,
il faudrait, pour faire ĂŠquilibre dans le plateau opposĂŠ, 580 000 cubes
de cuivre de 4 kilomètres de côtÊ [...]. Or, en supposant que l'oxygène
dĂŠgagĂŠ par les plantes
tout entière dans un ballon et suspendre celui-ci au plateau d'une balance,
il faudrait, pour faire ĂŠquilibre dans le plateau opposĂŠ, 580 000 cubes
de cuivre de 4 kilomètres de côtÊ [...]. Or, en supposant que l'oxygène
dÊgagÊ par les plantes compense seulement l'effet des causes d'absorption d'oxygène, autres que
celles qui sont le rĂŠsultat de la respiration des ĂŞtres vivants, au bout
d'un siècle, tout le genre humain et trois fois son Êquivalent n'auraient
absorbÊ qu'une quantitÊ d'oxygène Êgale à 15 ou 16 de ces cubes de
cuivre, tandis que l'air en renferme près de 134 000. 
compense seulement l'effet des causes d'absorption d'oxygène, autres que
celles qui sont le rĂŠsultat de la respiration des ĂŞtres vivants, au bout
d'un siècle, tout le genre humain et trois fois son Êquivalent n'auraient
absorbÊ qu'une quantitÊ d'oxygène Êgale à 15 ou 16 de ces cubes de
cuivre, tandis que l'air en renferme près de 134 000. 
-
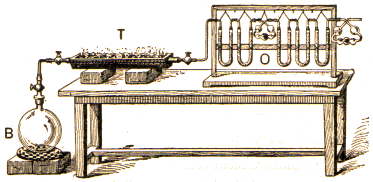
Appareil
utilisĂŠ par Dumas et Boussingault pour l'analyse de l'air en poids.
O.tubes
en U et tubes de Liebig pour la purification de
l'air.
T.
tube contenant le cuivre chauffĂŠ au rouge sombre.
B.
ballon ordinaire.
Aux constituants de l'atmosphère dÊjà mentionnÊes,
les physiciens et les chimistes ont ajoutĂŠ une multitude d'autres corps
plus ou moins perceptibles. Voici les plus importants :
1° l'acide carbonique, qui se
trouve toujours dans le rapport de 3 litres en moyenne pour 10 000 litres
d'air;
2° l'ammoniaque, surtout à l'Êtat de
carbonate, une petite quantitĂŠ ĂŠtant Ă l'ĂŠtat d'azotate et peut-ĂŞtre
Ă l'ĂŠtat d'azotite d'ammoniaque (Schoenbein);
3° la vapeur d'eau, toujours prÊsente,
mais en proportion très variable, suivant la tempÊrature et les saisons;
4° l'ozone,
molÊcule composÊe de trois atomes d'oxygène, dÊcouverte à Bâle dans
les annĂŠes 1840 par ShĂśnbein (Shoenbein),
qui, lui constatant une forte rÊactivitÊ chimique, y vit très tôt un
polluant;
5° des substances hydrocarbonÊs, principalement
de petites quantitĂŠs de gaz des marais;
6° l'iode, mÊtalloïde qui existe normalement
dans l'air, mais en très faibles proportions (Cahtin);
7° des matières salines, comme le chlorure
de sodium, le sulfate de soude. En effet, que l'on ouvre un ballon contenant
une dissolution
sursaturĂŠe de sulfate de soude, le plus souvent la cristallisation
sera instantanÊe; or, cette dernière est dÊterminÊe par la prÊsence
d'une trace de sulfate de soude (Gernez);
8° des poussières et des germes vivants
(pollens ,
bactĂŠries ,
bactĂŠries ,
etc.), corps qui sont d'autant plus rares que l'on s'Êlève davantage
dans l'atmosphère (Pasteur). ,
etc.), corps qui sont d'autant plus rares que l'on s'Êlève davantage
dans l'atmosphère (Pasteur).
Ajoutons, qu'entre 1895
et 1900 ont ĂŠtĂŠ mis en ĂŠvidence,
par distillation fractionnĂŠe de l'air liquide, d'autres composants de
l'air : l'argon, l'hĂŠlium, le nĂŠon, le krypton et le xĂŠnon, surnommĂŠs
gaz
rares, parce qu'ils se trouvent en quantitÊs très faibles dans l'atmosphère.
(Hoefer
/ Bourgoin). |
|