 |
La
radioactivitÃĐ
est le processus par lequel un noyau atomique
instable se transforme spontanÃĐment en un autre noyau plus stable, en
ÃĐmettant des particules ou un rayonnement. Elle rÃĐsulte de l'ÃĐquilibre
prÃĐcaire entre les forces nuclÃĐaires et ÃĐlectromagnÃĐtiques à l'intÃĐrieur
du noyau.
Les types de radioactivitÃĐ.
Plusieurs types
de dÃĐsintÃĐgrations existent, chacun caractÃĐrisÃĐ par une nature spÃĐcifique
des particules ÃĐmises et par des changements
dans la composition du noyau. Les principaux sont la radioactivitÃĐ alpha
(ÃĐmission d'un noyau d'hÃĐlium), bÊta (ÃĐmission
d'un ÃĐlectron ou d'un positon)
et gamma (ÃĐmission de photons de trÃĻs haute
ÃĐnergie). Ces trois grands types de radioactivitÃĐ sont frÃĐquemment associÃĐs
entre eux dans les chaÃŪnes de dÃĐsintÃĐgration des noyaux lourds. Ils
traduisent la recherche par le noyau d'un ÃĐtat plus stable, Ã travers
des transformations successives.
RadioactivitÃĐ
alpha.
La radioactivitÃĐ
alpha (Îą) est une des formes les plus anciennes et les plus faciles Ã
dÃĐtecter est. Dans ce cas, le noyau ÃĐjecte une particule Îą, qui correspond
à un noyau d'hÃĐlium 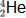 ,
formÃĐ de deux protons et de deux neutrons.
Cette ÃĐmission diminue le nombre de masse du noyau de quatre unitÃĐs et
son numÃĐro atomique de deux, entraÃŪnant une transmutation en un ÃĐlÃĐment
chimique diffÃĐrent. Par exemple : ,
formÃĐ de deux protons et de deux neutrons.
Cette ÃĐmission diminue le nombre de masse du noyau de quatre unitÃĐs et
son numÃĐro atomique de deux, entraÃŪnant une transmutation en un ÃĐlÃĐment
chimique diffÃĐrent. Par exemple :
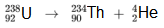
Ce type de dÃĐsintÃĐgration
concerne principalement les noyaux lourds (Z > 83) dans lesquels la rÃĐpulsion
ÃĐlectrostatique entre protons devient trop forte pour Être compensÃĐe
par la force nuclÃĐaire. Les particules alpha, bien que massives et fortement
chargÃĐes, possÃĻdent un faible pouvoir de pÃĐnÃĐtration, se limitant Ã
quelques centimÃĻtres dans l'air ou à une simple feuille de papier.
RadioactivitÃĐ
bÊta.
La radioactivitÃĐ
bÊta (Îēâŧ/Îēâš) se produit lorsqu'un excÃĻs de neutrons ou de protons
dÃĐsÃĐquilibre le noyau.
Dans la dÃĐsintÃĐgration
bÊta nÃĐgative (Îēâ), un neutron se transforme en proton,
tout en ÃĐmettant un ÃĐlectron et un antineutrino ÃĐlectronique :
nâ
ââ
âââ
ââ
âp
+ eâ +  .
.
Ce processus, qui
vise à abaisser un rapport N/Z trop ÃĐlevÃĐ, augmente le numÃĐro atomique
de 1 sans modifier le nombre de masse, car un neutron est remplacÃĐ par
un proton. à l'inverse, dans la dÃĐsintÃĐgration bÊta positive (Îē+),
qui permet d'augmenter unrapport N/Z trop faible, un proton se convertit
en neutron avec ÃĐmission d'un positon et d'un neutrino
selon :
pâ
ââ
âââ
ââ
ân
+ e+ + . .
â
Il existe ÃĐgalement
la capture ÃĐlectronique, oÃđ le noyau absorbe un ÃĐlectron des couches
atomiques, transformant un proton en neutron. Dans tous les cas, la radioactivitÃĐ
bÊta permet d'ajuster le rapport entre neutrons et protons vers une configuration
plus stable. Les particules bÊta, plus lÃĐgÃĻres que les particules alpha,
possÃĻdent un pouvoir de pÃĐnÃĐtration plus grand, pouvant traverser quelques
millimÃĻtres de mÃĐtal lÃĐger.
RadioactivitÃĐ
gamma.
Un noyau excitÃĐ
peut ÃĐgalement se dÃĐsexciter par ÃĐmission d'un rayonnement
ÃĐlectromagnÃĐtique de haute ÃĐnergie. Cela correspond à la radioactivitÃĐ
gamma (Îģ). Dans ce cas, aucun changement de nature chimique n'a lieu,
car ni le nombre de masse ni le numÃĐro atomique ne sont modifiÃĐs. Le
noyau libÃĻre simplement un excÃĻs d'ÃĐnergie
sous forme de photons gamma, souvent aprÃĻs une dÃĐsintÃĐgration alpha
ou bÊta. Les rayonnements gamma sont extrÊmement pÃĐnÃĐtrants et nÃĐcessitent
des ÃĐcrans ÃĐpais de plomb ou de bÃĐton pour Être attÃĐnuÃĐs.
Autres
modes de dÃĐsintÃĐgration.
En plus des trois
formes classiques de radioactivitÃĐ, il existe des modes de dÃĐsintÃĐgration
plus rares, qui impliquent principalement certains noyaux trÃĻs riches
en protons ou en neutrons, ou des noyaux trÃĻs lourds.
âĒ RadioactivitÃĐ
proton et radioactiovitÃĐ neutron. - Dans certains cas, un noyau instable
peut ÃĐmettre directement un proton. Cette radioactivitÃĐ proton apparaÃŪt
dans les noyaux proches de la limite de stabilitÃĐ pour les protons, lÃ
oÃđ la rÃĐpulsion ÃĐlectrostatique devient trÃĻs forte. L'ÃĐmission de
proton rÃĐduit le numÃĐro atomique de 1, le nombre de masse est diminuÃĐ
d'une unitÃĐ. C'est un phÃĐnomÃĻne relativement rare, observÃĐ dans des
isotopes artificiels produits en laboratoire. Ã l'opposÃĐ, certains noyaux
riches en neutrons peuvent ÃĐjecter un neutron. La radioactivitÃĐ neutron
conduit alors à une diminution du nombre de masse d'une unitÃĐ, sans modification
du numÃĐro atomique. Ce type de dÃĐsintÃĐgration est plus frÃĐquent dans
des noyaux exotiques crÃĐÃĐs dans les accÃĐlÃĐrateurs.
âĒ RadioactivitÃĐ
diproton. - Une autre forme de dÃĐsintÃĐgration particuliÃĻre est l'ÃĐmission
de particule double, comme l'ÃĐmission de deux protons simultanÃĐment,
appelÃĐe radioactivitÃĐ diproton ou radioactivitÃĐ 2-protons). Elle se
produit lorsque l'ÃĐmission simultanÃĐe est plus favorable que l'ÃĐmission
successive, en raison de barriÃĻres ÃĐnergÃĐtiques. Ces processus restent
rares et constituent surtout des sujets d'ÃĐtude pour la physique des noyaux
trÃĻs instables.
âĒ Double dÃĐsintÃĐgration
bÊta. - Un autre phÃĐnomÃĻne rare mais thÃĐoriquement possible est
la double dÃĐsintÃĐgration bÊta. Dans ce processus, deux neutrons d'un
mÊme noyau se transforment simultanÃĐment en deux protons, avec ÃĐmission
de deux ÃĐlectrons et de deux antineutrinos. L'ÃĐquation s'ÃĐcrit : (Z,
A)â
ââ
âââ
ââ
â(Z+2, A) + 2eâ + 2 .
Ce processus est extrÊmement lent et n'a ÃĐtÃĐ observÃĐ que dans certains
isotopes particuliers, comme le germanium 76 ou le xÃĐnon 136. Il existe
ÃĐgalement une hypothÃĻse encore plus fondamentale, celle de la double
bÊta sans ÃĐmission de neutrinos, qui permettrait de vÃĐrifier si le neutrino
est sa propre antiparticule (particule de Majorana). Dans le mÊme ordre
d'idÃĐes, notons qu'il pourrait aussi exister une forme de dÃĐsintÃĐgration
double par l'ÃĐmission de deux particules alpha. .
Ce processus est extrÊmement lent et n'a ÃĐtÃĐ observÃĐ que dans certains
isotopes particuliers, comme le germanium 76 ou le xÃĐnon 136. Il existe
ÃĐgalement une hypothÃĻse encore plus fondamentale, celle de la double
bÊta sans ÃĐmission de neutrinos, qui permettrait de vÃĐrifier si le neutrino
est sa propre antiparticule (particule de Majorana). Dans le mÊme ordre
d'idÃĐes, notons qu'il pourrait aussi exister une forme de dÃĐsintÃĐgration
double par l'ÃĐmission de deux particules alpha.
âĒ Fission spontanÃĐe.
- Pour les noyaux trÃĻs lourds, proches de la limite supÃĐrieure du tableau
pÃĐriodique, on observe un mode de dÃĐsintÃĐgration appelÃĐ fission spontanÃĐe.
Le noyau, au lieu d'ÃĐmettre une petite particule, se scinde en deux fragments
de taille comparable, accompagnÃĐs de l'ÃĐmission de neutrons et d'une
grande quantitÃĐ d'ÃĐnergie. Contrairement à la fission induite par des
neutrons (utilisÃĐe dans les rÃĐacteurs), la fission spontanÃĐe survient
sans dÃĐclenchement externe. Elle devient de plus en plus probable lorsque
le noyau contient un grand nombre de protons et de neutrons, comme c'est
le cas pour l'uranium, le plutonium ou les ÃĐlÃĐments transuraniens.
Loi de dÃĐcroissance
radioactive.
La loi de dÃĐcroissance
radioactive dÃĐcrit la vitesse à laquelle un nombre donnÃĐ de noyaux atomiques
instables se dÃĐsintÃĻgrent de maniÃĻre alÃĐatoire et spontanÃĐe. Elle
ÃĐtablit que le taux de dÃĐsintÃĐgration, c'est-Ã -dire le nombre de dÃĐsintÃĐgrations
par unitÃĐ de temps, est proportionnel au nombre de noyaux radioactifs
prÃĐsents à l'instant considÃĐrÃĐ.
MathÃĐmatiquement,
cette probabilitÃĐ s'exprime par une ÃĐquation diffÃĐrentielle. Si l'on
note N(t) le nombre de noyaux radioactifs à l'instant t et Îŧ la constante
radioactive (caractÃĐristique du nuclÃĐide considÃĐrÃĐ), la loi s'ÃĐcrit
: dN(t)/dt = âÎŧN(t). Le signe nÃĐgatif indique que N(t) diminue avec
le temps. La rÃĐsolution de cette ÃĐquation
diffÃĐrentielle conduit à la fonction
exponentielle dÃĐcroissante qui est la forme la plus courante pour
exprimer la loi : N(t) = N0eâÎŧt.
Dans cette expression, N0â reprÃĐsente le nombre
initial de noyaux radioactifs à l'instant t = 0.
La loi de dÃĐcroissance
radioactive est statistique par nature. Il est impossible de prÃĐdire Ã
quel moment prÃĐcis un noyau individuel se dÃĐsintÃĐgrera; on ne peut que
donner une probabilitÃĐ de dÃĐsintÃĐgration sur une pÃĐriode donnÃĐe. La
constante Îŧ reprÃĐsente prÃĐcisÃĐment cette probabilitÃĐ de dÃĐsintÃĐgration
par unitÃĐ de temps pour un noyau. La dÃĐcroissance exponentielle n'est
donc valable et observable que pour un trÃĻs grand nombre de noyaux, oÃđ
les fluctuations statistiques deviennent nÃĐgligeables.
Cette loi permet
ÃĐgalement de dÃĐfinir l'activitÃĐ A(t) d'une source radioactive, qui correspond
au nombre de dÃĐsintÃĐgrations par seconde. Elle est mesurÃĐe en becquerels
(Bq). L'activitÃĐ suit la mÊme dÃĐcroissance exponentielle que le nombre
de noyaux : A(t) = âdN/dt = ÎŧN(t) = N0eâÎŧt
=
A0eâÎŧt, oÃđ A0
= ÎŧN0â est l'activitÃĐ initiale à t = 0.
Une autre grandeur
essentielle, plus concrÃĻte, est la pÃĐriode radioactive, ou demi-vie,
notÃĐe T. Il s'agit du temps nÃĐcessaire pour que la moitiÃĐ des noyaux
radioactifs prÃĐsents se dÃĐsintÃĻgrent. On peut la relier à la constante
radioactive Îŧ en posant N(T)=N0/2 dans la solution
de la loi. On obtient alors : N0/2 = N0eâÎŧt.
En simplifiant et en prenant le logarithme
nÃĐpÃĐrien, on trouve la relation : lnâĄ(1/2)=âÎŧT, soit T = lnâĄ(2)/Îŧ.
Datation radioactive.
DiffÃĐrentes techniques
utilisent la dÃĐsintÃĐgration radioactive de certains isotopes pour de
dÃĐterminer l'ÃĒge des matÃĐriaux naturels. Parmi elles, on peut citer
la mÃĐthode du carbone-14 qui est particuliÃĻrement
utilisÃĐe pour dater des matÃĐriaux organiques, comme le bois ou les ossements,
jusqu'Ã environ 50 000 ans. La mÃĐthode du potassium-argon et de ses dÃĐrivÃĐs
(argon-argon) est employÃĐe pour dater des roches volcaniques et des minÃĐraux
anciens, pouvant atteindre des millions d'annÃĐes. La mÃĐthodologie de
l'uranium-thorium repose sur la transformation successive de l'uranium-238
en thorium-230, ce qui est utile pour dater les calcites, stalactites ou
coraux. Enfin, les techniques de l'uranium-plomb et du rubidium-strontium
sont d'autres mÃĐthodes largement utilisÃĐes pour dater des roches anciennes,
avec un potentiel d'application jusqu'Ã plusieurs milliards d'annÃĐes.
Carbone-14.
La mÃĐthode du carbone-14
est largement utilisÃĐe pour dater des matÃĐriaux organiques, comme le
bois, les ossements, les tissus ou les charbons, remontant à quelques
centaines d'annÃĐes jusqu'Ã environ 50 000 ans. Le carbone-14 est un isotope
radioactif du carbone, produit naturellement dans l'atmosphÃĻre par le
rayonnement
cosmique qui bombarde les nuages de particules chargÃĐes. Ce rayonnement
transforme une partie des atomes de carbone-12 en carbone-14. Le carbone-14
est ensuite assimilÃĐ par les organismes vivants via l'air et l'eau, en
proportion avec le carbone-12 stable. Une fois l'organisme mort, l'absorption
de carbone-14 cesse et le carbone-14 prÃĐsent dans le corps commence Ã
se dÃĐsintÃĐgrer en azote-14, suivant une demi-vie de 5730 ans. La dÃĐsintÃĐgration
radioactive du carbone-14 est rÃĐguliÃĻre et prÃĐvisible, ce qui permet
de dÃĐterminer l'ÃĒge d'un ÃĐchantillon en mesurant la proportion de carbone-14
restant par rapport au carbone-12.
Pour effectuer une
datation
au carbone-14, un ÃĐchantillon de matiÃĻre organique est collectÃĐ et traitÃĐ
pour isoler les composÃĐs contenant du carbone. Des techniques comme la
combustion pour les tissus ou l'acide phosphorique pour les ossements peuvent
Être utilisÃĐes pour extraire le carbone. L'ÃĐchantillon est ensuite analysÃĐ
par spectromÃĐtrie de masse ou par comptage par dÃĐtecteur de particules
alpha ou beta. Ces mÃĐthodes permettent de mesurer la concentration relative
de carbone-14 et de carbone-12.
Il existe ÃĐgalement
une version amÃĐliorÃĐe de cette technique appelÃĐe datation au carbone-14
AMS (Accelerator Mass Spectrometry), qui permet de mesurer des concentrations
de carbone-14 beaucoup plus faibles et donc d'ÃĐtendre la plage d'ÃĒge
des ÃĐchantillons jusqu'Ã environ 60 000 ans. Cette mÃĐthode est particuliÃĻrement
prÃĐcise pour les ÃĐchantillons contenant de petites quantitÃĐs de carbone.
Bien que la datation
au carbone-14 soit une mÃĐthode puissante, elle prÃĐsente certaines limitations.
Par exemple, les niveaux de carbone-14 dans l'atmosphÃĻre ont fluctuÃĐ
au cours du temps en raison des variations solaires ou des changements
climatiques. Pour compenser cela, des corrections sont appliquÃĐes en utilisant
des courbes de calibration basÃĐes sur des sÃĐries temporelles de donnÃĐes
provenant de sources indÃĐpendantes, comme les anneaux de croissance des
arbres ou les couches de glace polaires.
Potassium-argon.
Argon-argon.
La mÃĐthode du potassium-argon
et son dÃĐrivÃĐ, la mÃĐthode de l'argon-argon, sont des techniques spÃĐcialement
appropriÃĐes pour dater des roches volcaniques
et des minÃĐraux anciens. Le potassium-40, prÃĐsent naturellement dans
les roches, est un isotope instable qui se dÃĐsintÃĻgre en argon-40, un
gaz
inerte. Lorsque la roche est formÃĐe, elle contient une quantitÃĐ fixe
de potassium-40. Avec le temps, une partie de ce potassium
se transforme en argon-40, qui reste emprisonnÃĐ dans la roche. En mesurant
la quantitÃĐ de potassium-40 restant et celle d'argon-40 produit, il est
possible de calculer l'ÃĒge de la roche. La mÃĐthode argon-argon
utilise une ÃĐtape supplÃĐmentaire de chauffage de l'ÃĐchantillon sous
un flux de neutrons pour convertir une partie du potassium-39 en argon-39.
Cela permet de mieux calibrer et de rÃĐduire les erreurs dans la mesure
du rapport entre potassium-40 et argon-40, offrant ainsi une prÃĐcision
accrue dans la datation. La mÃĐthode potassium-argon est particuliÃĻrement
efficace pour dater des ÃĐchantillons ayant entre 100 000 et plusieurs
millions d'annÃĐes. La mÃĐthode argon-argon permet de dater des ÃĐchantillons
encore plus anciens, jusqu'Ã plusieurs milliards d'annÃĐes, en fournissant
des rÃĐsultats plus fiables et plus prÃĐcis que la mÃĐthode potassium-argon
classique.
Uranium-thorium.
La mÃĐthode uranium-thorium
est utilisÃĐe pour dater des matÃĐriaux riches en ÃĐlÃĐments du groupe
des actinides, comme les calcites, les coraux
ou les stalactites. L'uranium-238, prÃĐsent
naturellement dans ces matÃĐriaux, subit une sÃĐrie de dÃĐsintÃĐgrations
radioactives pour former finalement du plomb 206. Tout au long de cette
chaÃŪne de dÃĐsintÃĐgration, diffÃĐrents isotopes intermÃĐdiaires sont
produits, notamment le thorium-230. Ce dernier est particuliÃĻrement important
car il se sÃĐpare chimiquement de l'uranium, accumulant progressivement
dans le matÃĐriau. En mesurant la proportion de thorium-230 par rapport
à l'uranium-234 dans un ÃĐchantillon, il est possible de calculer son
ÃĒge. Cette mÃĐthode est trÃĻs prÃĐcise pour des ÃĐchantillons ÃĒgÃĐs de
plusieurs centaines d'annÃĐes à plusieurs centaines de milliers d'annÃĐes.
Elle est particuliÃĻrement utile pour dater des phÃĐnomÃĻnes gÃĐologiques
ou archÃĐologiques impliquant des matÃĐriaux carbonatÃĐs ou calcifiÃĐs.
Uranium-plomb.
La mÃĐthode uranium-plomb
est fondÃĐe sur la dÃĐsintÃĐgration de l'uranium-238 en plomb-206 et de
l'uranium-235 en plomb-207. Ces deux isotopes d'uranium, prÃĐsents naturellement
dans de nombreux minÃĐraux comme le zircon,
subissent une sÃĐrie de dÃĐsintÃĐgrations radioactives au fil du temps.
Chaque isotope a sa propre demi-vie : environ 4,47 milliards d'annÃĐes
pour l'uranium 238 et 704 millions d'annÃĐes pour l'uranium-235. En mesurant
la proportion de chaque isotope d'uranium restant et de plomb formÃĐ dans
un ÃĐchantillon, il est possible de calculer son ÃĒge avec une grande prÃĐcision.
Cette mÃĐthode est particuliÃĻrement efficace pour dater des ÃĐchantillons
anciens, allant jusqu'Ã plusieurs milliards d'annÃĐes. Elle est couramment
utilisÃĐe pour ÃĐtudier l'histoire gÃĐologique
de la Terre dans le contexte de la formation des cristaux
minÃĐraux ou des roches ignÃĐes.
Rubidium-strontium.
La mÃĐthode rubidium-strontium
est basÃĐe sur la dÃĐsintÃĐgration de l'isotope radioactif du rubidium-87
en strontium-87. Le rubidium-87 est prÃĐsent naturellement dans de nombreux
minÃĐraux comme le mica, le biotite et le muscovite.
Lors de la formation de la roche, le rubidium-87 est homogÃĻne dans l'ÃĐchantillon.
Au fil du temps, une partie de ce rubidium se dÃĐsintÃĻgre en strontium-87,
qui s'accumule dans le matÃĐriau. En mesurant la proportion de rubidium-87
restant et de strontium-87 formÃĐ, il est possible de calculer l'ÃĒge de
la roche. Cette mÃĐthode est particuliÃĻrement adaptÃĐe pour dater des
ÃĐchantillons anciens, allant jusqu'Ã plusieurs milliards d'annÃĐes. Elle
est souvent utilisÃĐe pour ÃĐtudier la thermochronologie, c'est-Ã -dire
la maniÃĻre dont les roches ont refroidi et ÃĐvoluÃĐ depuis leur formation.
La mÃĐthode rubidium-strontium est ÃĐgalement utilisÃĐe pour dater des
ÃĐvÃĐnements gÃĐologiques importants, tels que les collisions de plaques
tectoniques ou les ÃĐruptions volcaniques.
Les familles radioactives.
Une famille radioactive
( = sÃĐrie radioactive), est un ensemble d'ÃĐlÃĐments chimiques radioactifs
qui sont liÃĐs les uns aux autres par une chaÃŪne de dÃĐsintÃĐgrations.
Le processus commence avec un radioisotope particulier, appelÃĐ parent,
qui est instable. Pour atteindre une forme plus stable, il se dÃĐsintÃĻgre
en ÃĐmettant des rayonnements (comme une particule alpha ou bÊta) et se
transforme en un nouvel ÃĐlÃĐment, appelÃĐ fils ou descendant. Ce nouvel
ÃĐlÃĐment, ou isotope, est souvent lui-mÊme radioactif et instable. Il
va donc à son tour se dÃĐsintÃĐgrer en un autre ÃĐlÃĐment, et ainsi de
suite. Cette succession de transformations se poursuit ÃĐtape par ÃĐtape
jusqu'à ce qu'elle aboutisse finalement à un isotope stable, qui ne se
dÃĐsintÃĻgre plus. Ce dernier ÃĐlÃĐment est le terme stable de la sÃĐrie.
Il existe quatre
familles radioactives naturelles principales qui correspondent à des chaÃŪnes
de dÃĐsintÃĐgrations successives issues de noyaux lourds instables prÃĐsents
dans la croÃŧte terrestre. Chaque famille dÃĐbute par un isotope à trÃĻs
longue pÃĐriode, se poursuit par une sÃĐrie de transformations Îą et Îēâŧ,
et se termine sur un isotope stable du plomb ou
du bismuth. Elles se distinguent par le nombre
de masse des noyaux impliquÃĐs, qui obÃĐit à une congruence modulaire
particuliÃĻre, et par les isotopes caractÃĐristiques rencontrÃĐs au cours
de la chaÃŪne. Dans l'ensemble, ces quatre familles traduisent l'organisation
rÃĐguliÃĻre des dÃĐsintÃĐgrations Îą et Îē dans les noyaux lourds. Elles
expliquent la prÃĐsence conjointe de plusieurs isotopes dans les minerais
radioactifs, structurent l'histoire de la radioactivitÃĐ terrestre et jouent
un rÃīle fondamental dans la datation gÃĐologique, la radioprotection et
la comprÃĐhension de l'ÃĐvolution des ÃĐlÃĐments dans la nature.
SÃĐrie
du thorium.
La premiÃĻre famille,
appelÃĐe parfois sÃĐrie du thorium, correspond à la suite des noyaux dont
le nombre de masse est divisible par 4. Elle dÃĐbute par le thorium-232,
dont la demi-vie est de l'ordre de 14 milliards d'annÃĐes, soit comparable
à l'ÃĒge de la Terre. Ce noyau subit une succession de dÃĐsintÃĐgrations
Îą et Îēâŧ, produisant notamment le radium-228, l'actinium-228 et divers
isotopes du radon et du polonium, avant de s'achever sur le plomb-208 stable.
SÃĐrie
de l'uranium.
La deuxiÃĻme famille,
connue sous le nom de sÃĐrie de l'uranium-radium, rassemble les noyaux
dont le nombre de masse est de la forme 4n+2. Elle commence par l'uranium-238,
isotope primordial dont la demi-vie est d'environ 4,5 milliards d'annÃĐes.
Sa chaÃŪne est l'une des plus ÃĐtudiÃĐes en raison de l'importance du radon-222,
gaz radioactif ÃĐmanant du sol, et des isotopes du radium, longtemps utilisÃĐs
en radiothÃĐrapie. Les dÃĐsintÃĐgrations multiples mÃĻnent finalement au
plomb-206 stable.
SÃĐrie
de l'actinium.
La troisiÃĻme famille,
dite sÃĐrie de l'actinium, correspond aux noyaux de la forme 4n+3. Elle
est initiÃĐe par l'uranium-235, isotope fissile dont la demi-vie avoisine
700 millions d'annÃĐes. Sa chaÃŪne comprend le thorium-231, le protactinium-231,
ainsi que des descendants tels que le radon-219 et plusieurs isotopes du
polonium et du bismuth. Cette sÃĐrie se termine sur le plomb-207 stable.
Bien que moins abondante que celle de l'uranium-238, elle joue un rÃīle
central en physique nuclÃĐaire en raison de l'importance de l'uranium-235
dans les rÃĐacteurs et les armes nuclÃĐaires.
SÃĐrie
du neptunium.
La quatriÃĻme famille,
appelÃĐe sÃĐrie du neptunium, regroupe les noyaux de la forme 4n+1. Elle
devrait thÃĐoriquement dÃĐbuter par le neptunium-237, isotope artificiel,
mais dans la nature, cette famille ÃĐtait autrefois reprÃĐsentÃĐe par l'isotope
primordial plutonium-241 ou par des noyaux aujourd'hui disparus en raison
de leurs demi-vies relativement courtes à l'ÃĐchelle gÃĐologique. Ses
descendants incluent des isotopes du thorium, du protactinium et de l'uranium,
avant de s'achever sur le thallium-205 ou le bismuth-209 stable. Ã l'ÃĐpoque
actuelle, cette sÃĐrie n'est pratiquement plus observable dans les minÃĐraux
naturels, sauf à travers des traces infimes de noyaux produits par rÃĐactions
cosmiques ou artificiellement dans les rÃĐacteurs.
La radioactivitÃĐ
dans la vie.
La comprÃĐhension
scientifique de la radioactivitÃĐ a profondÃĐment marquÃĐ les sociÃĐtÃĐs
humaines depuis sa dÃĐcouverte, en ouvrant des perspectives technologiques
inÃĐdites mais aussi en soulevant des inquiÃĐtudes liÃĐes à la gestion
des dÃĐchets radioactifs, au risque d'accidents nuclÃĐaires et aux prÃĐoccupations
de sÃĐcuritÃĐ liÃĐes à la prolifÃĐration des armes nuclÃĐaires.
Dans le domaine mÃĐdical,
elle a permis de dÃĐvelopper la radiothÃĐrapie pour le traitement des cancers,
l'imagerie nuclÃĐaire grÃĒce aux traceurs radioactifs, et la stÃĐrilisation
de matÃĐriel mÃĐdical. Ces usages ont considÃĐrablement amÃĐliorÃĐ la prise
en charge des maladies graves et prolongÃĐ l'espÃĐrance de vie, au prix
d'une exposition contrÃīlÃĐe aux rayonnements.
Dans la recherche
scientifique, la radioactivitÃĐ est un outil prÃĐcieux. Elle a permis ,
on l'a vu, de dater par exemple les roches et de reconstituer l'histoire
de la Terre. Elle a aussi permis d'ÃĐtudier les mÃĐcanismes biologiques
à l'ÃĐchelle cellulaire, et de comprendre la
structure de la matiÃĻre grÃĒce aux isotopes traceurs. Ces usages renforcent
la connaissance humaine et soutiennent le dÃĐveloppement technologique
dans de nombreux secteurs.
Dans la vie quotidienne,
certaines applications plus discrÃĻtes se sont dÃĐveloppÃĐes : la conservation
des aliments par irradiation, les dÃĐtecteurs de fumÃĐe utilisant l'amÃĐricium-241,
ou encore les techniques industrielles de contrÃīle de qualitÃĐ et de mesure
par rayonnements. Ces usages banalisÃĐs rappellent que la radioactivitÃĐ
n'est pas seulement associÃĐe aux grandes mais aussi à des applications
les plus pratiques.
Impacts
sanitaires et environnementaux.
En contrepartie,
les impacts sur la santÃĐ publique et l'environnement sont significatifs.
Les effets de la
radioactivitÃĐ sur la santÃĐ et l'environnement dÃĐpendent de la dose reçue
et du type de rayonnement. Ã faibles doses, le corps humain peut rÃĐparer
une partie des dommages causÃĐs aux cellules, mais à fortes doses les
rayonnements ionisants peuvent provoquer des mutations, des brÃŧlures,
des cancers ou la mort cellulaire massive. L'exposition chronique à des
radionuclÃĐides naturels comme le radon constitue un risque pour les populations.
Les travailleurs du nuclÃĐaire, les patients soumis à des examens rÃĐpÃĐtÃĐs,
ou les habitants des zones contaminÃĐes par des essais ou des accidents
subissent des niveaux variables de rayonnement qui nÃĐcessitent une surveillance
stricte. La radioÃĐcologie s'attache à ÃĐtudier ces effets à long terme
sur les ÃĐcosystÃĻmes, montrant que les radionuclÃĐides
peuvent persister dans les sols et les chaÃŪnes alimentaires.
Les accidents nuclÃĐaires
sont l'illustration la plus spectaculaire des impacts sanitaires et environnementaux
de la radioactivitÃĐ. L'explosion du rÃĐacteur de Tchernobyl en 1986, en
Ukraine
(alors composante de l'URSS) a entraÃŪnÃĐ
un rejet massif de radionuclÃĐides dans l'atmosphÃĻre, contaminant durablement
de vastes territoires d'Ukraine, de BiÃĐlorussie
et de Russie. Le nuage radioactif s'est diffusÃĐ
sur l'Europe entiÃĻre, provoquant une ÃĐlÃĐvation
temporaire des taux de cÃĐsium-137 et d'iode-131. Les impacts immÃĐdiats
se sont traduits par des dÃĐcÃĻs dus au syndrome d'irradiation aiguÃŦ parmi
les liquidateurs, et à plus long terme par une augmentation significative
des cancers de la thyroÃŊde, notamment chez
les enfants exposÃĐs à l'iode radioactif. Sur l'environnement,
la zone d'exclusion demeure aujourd'hui un laboratoire naturel, oÃđ la
faune et la flore persistent malgrÃĐ une radioactivitÃĐ ambiante ÃĐlevÃĐe,
offrant un terrain d'ÃĐtude unique sur la rÃĐsilience ÃĐcologique.
En 2011, la catastrophe
de Fukushima, au Japon, a rappelÃĐ la vulnÃĐrabilitÃĐ
des installations face aux risques naturels. Le sÃĐisme et le tsunami ont
entraÃŪnÃĐ la fusion partielle de plusieurs rÃĐacteurs et le rejet d'importantes
quantitÃĐs de radionuclÃĐides dans l'air et l'ocÃĐan
Pacifique. Les consÃĐquences sanitaires directes ont ÃĐtÃĐ plus limitÃĐes
que celles de Tchernobyl grÃĒce à une ÃĐvacuation rapide, mais les effets
psychologiques et sociaux sur les populations dÃĐplacÃĐes sont considÃĐrables.
Sur le plan environnemental, la dispersion de cÃĐsium-137 dans les sols
agricoles et dans l'eau a nÃĐcessitÃĐ une vaste campagne de dÃĐcontamination,
et l'impact sur les ÃĐcosystÃĻmes marins reste suivi de prÃĻs.
à une ÃĐchelle plus
diffuse, l'exposition au radon constitue aujourd'hui le premier facteur
de risque radiologique d'origine naturelle pour les populations. Ce gaz
radioactif, issu de la dÃĐsintÃĐgration de l'uranium dans les sols, peut
s'accumuler dans les habitations mal ventilÃĐes. L'inhalation de ses descendants
solides accroÃŪt significativement le risque de cancer du poumon, en particulier
chez les fumeurs. Dans certaines rÃĐgions granitiques ou volcaniques, comme
le Massif central, mais aussi en Bretagne
ou certaines zones d'AmÃĐrique du Nord,
ce danger invisible fait l'objet de campagnes de mesure et de prÃĐvention.
La gestion des dÃĐchets
radioactifs reprÃĐsente une autre dimension majeure des impacts à long
terme. Les dÃĐchets de haute activitÃĐ et à vie longue, issus principalement
des combustibles usÃĐs des centrales, contiennent des isotopes comme le
plutonium-239 ou l'amÃĐricium-241, dont les demi-vies se comptent en milliers
d'annÃĐes. Leur stockage gÃĐologique profond est envisagÃĐ comme solution,
mais il soulÃĻve des interrogations ÃĐthiques et pratiques : comment garantir
la sÃŧretÃĐ sur des temps si longs, comment transmettre la mÃĐmoire du
danger aux sociÃĐtÃĐs futures, et comment ÃĐviter tout risque de dissÃĐmination?
L'environnement terrestre
et marin garde aussi la trace des essais nuclÃĐaires atmosphÃĐriques rÃĐalisÃĐs
entre 1945 et 1980 ( PolynÃĐsie
française, Atoll Johnston). Ces explosions
expÃĐrimentales ont diffusÃĐ du strontium-90 et du cÃĐsium-137 sur toute
la planÃĻte, mesurables encore aujourd'hui dans les sols, les glaces et
parfois dans les organismes vivants. Ces retombÃĐes constituent une archive
involontaire de l'ÃĻre nuclÃĐaire, qui a modifiÃĐ de façon durable la
radioactivitÃĐ de fond terrestre. PolynÃĐsie
française, Atoll Johnston). Ces explosions
expÃĐrimentales ont diffusÃĐ du strontium-90 et du cÃĐsium-137 sur toute
la planÃĻte, mesurables encore aujourd'hui dans les sols, les glaces et
parfois dans les organismes vivants. Ces retombÃĐes constituent une archive
involontaire de l'ÃĻre nuclÃĐaire, qui a modifiÃĐ de façon durable la
radioactivitÃĐ de fond terrestre. |
|