| . |
|
||||||
|
|
| . |
|
||||||
| La physique > ElectromagnÃĐtisme |
Aperçu |
Le mot spectre
revÊt en physique plusieurs sens. EmployÃĐ
dans son acception la plus large, il dÃĐsigne un ensemble de radiations
monochromatiques d'un type particulier. Ainsi, dans le contexte de l'ÃĐtude
du rayonnement
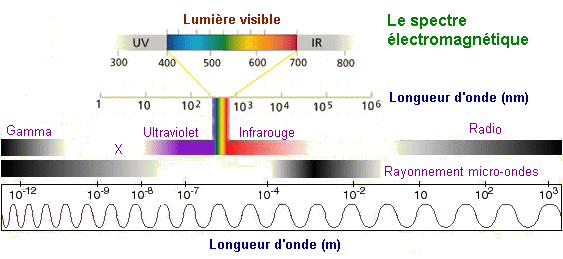
ÃĐlectromagnÃĐtique. On pourra alors parler de spectre ÃĐlectromagnÃĐtique
pour dÃĐsigner toute l'ÃĐtendue de la gamme de rayonnements ÃĐlectromagnÃĐtiques
possibles. Cet ensemble ÃĐtant couramment divisÃĐ en plusieurs parties
ou domaines. Ces domaines vont du rayonnement gamma,
dÃĐfini par des ÃĐnergies et des frÃĐquences
trÃĻs ÃĐlevÃĐes (soit par des longueurs d'ondes
trÃĻs courtes), au rayonnement radio, qui correspond
à des ÃĐnergies transportÃĐes par chacun de ses photons
trÃĻs faibles. La lumiÃĻre visible, encadrÃĐe par le rayonnement ultraviolet
(UV) et l'infrarouge (IR) correspondant pour
sa part à un domaine intermÃĐdiaire du spectre.
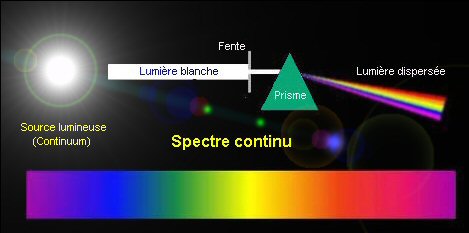
 Le mot spectre sert plus spÃĐcialement à dÃĐsigner la distribution d'une caractÃĐristique telle que l'intensitÃĐ d'un rayonnement (ou d'une onde quelconque), en fonction de son ÃĐnergie (ou d'une grandeur qui en dÃĐpend comme la frÃĐquence ou la longueur d'onde). On dÃĐsigne ainsi sous le nom de spectre lumineux la rÃĐpartition de l'intensitÃĐ d'une lumiÃĻre en fonction de la longueur d'onde (ou de la frÃĐquence) des rayonnements qu'elle contient. D'un point de vue plus concret, cela revient à dÃĐfinir un spectre comme l'apparence de la lumiÃĻre ÃĐmise par un corps lorsqu'elle est dispersÃĐe par un prisme (ou un rÃĐseau de diffraction). On reconnaÃŪtra alors trois familles principales de spectres : les spectres continus, oÃđ les diffÃĐrentes couleurs observÃĐes forment un continuum; les spectres de raies, qui sont eux-mÊmes de deux sortes : les spectres en absorption, oÃđ certaines radiations (signalÃĐes dans le dispositif expÃĐrimental par des raies sombres) sont absentes ou trÃĻs attÃĐnuÃĐes, et les spectres en ÃĐmission oÃđ, au contraire, certaines radiations (signalÃĐes dans le dispositif expÃĐrimental par des raies brillantes) sont plus intenses. L'explication des particularitÃĐs des spectres se trouve dans le caractÃĻre quantique des atomes, et plus spÃĐcialement de leur enveloppe ÃĐlectronique.
|
|||||||||||||||
Mise en ordre |
Les
spectres continus
Les corps solides
et les gaz trÃĻs comprimÃĐs portÃĐs à haute tempÃĐrature
(par exemple, un fer chauffÃĐ au rouge, ou les parties profondes de la
photosphÃĻre
des ÃĐtoiles) sont à l'origine d'un rayonnement continu,
que l'on appelle rayonnement thermique ou rayonnement de corps
noir. Ces caractÃĐristiques sont indÃĐpendantes de la composition chimique
de la source, et sont seulement fonction de sa tempÃĐrature, autrement
dit des ÃĐnergies impliquÃĐes. Plus un corps lumineux est chaud, et plus
son spectre continu contient de rayonnements bleus (cÃītÃĐ le plus ÃĐnergÃĐtique
du spectre), moins il est chaud, et plus sa couleur se rapprochera du rouge.
C'est ainsi que l'on peut avoir une idÃĐe de la tempÃĐrature superficielle
des ÃĐtoiles au simple constat de leur couleur. Ajoutons que le rayonnement
cosmologique, diffusÃĐ quelque centaines de milliers d'annÃĐes aprÃĻs
le big bang, a ÃĐgalement un spectre de corps
noir. Son maximum de rayonnement se situe à l'heure actuelle dans le domaine
micro-ondes, ce qui correspond à une tempÃĐrature de 3K.
 Outre celui du rayonnement de corps
noir, les spectres continus sont caractÃĐristiques de plusieurs sortes
de types de rayonnements. On citera le rayonnement synchrotron
et le rayonnement Cerenkov, le rayonnement Compton
et Compton inverse, et le rayonnement free-free.
Chacun des spectres correspondant possÃĻde un profil diffÃĐrent, ce qui
permet en gÃĐnÃĐral de l'identifier.
Les spectres de raies Lorsqu'on disperse un rayonnement lumineux pour former un spectre, on constate dans de nombreux cas (notamment lorsqu'il s'agit de rayonnements astronomiques) que des radiations, correspondant à certaines longueurs d'ondes ou frÃĐquences sont plus faible, voire absentes, et que d'autres en revanche sont trÃĻs intenses. Cela se traduit sur le spectre sous forme de raies sombres (raies en absorption) ou brillantes (raies en ÃĐmission) respectivement. Les conditions de tempÃĐrature et de pression, ainsi que la prÃĐsence ou non de champs magnÃĐtiques et ÃĐlectriques influent sur les caractÃĐristiques d'un tel spectre. Certaines raies peuvent Être plus ou moins larges, plus ou moins floues, elles sont parfois dÃĐdoublÃĐes. Mais ce qui le paramÃĻtre fondamental est la composition chimique du gaz impliquÃĐ. La succession de ces raies forment des ensembles ou systÃĻmes qui sont d'abord caractÃĐristiques des ÃĐlÃĐments chimiques responsables de l'ÃĐmission (ou de l'absorption) des radiations concernÃĐes. Et c'est donc seulement secondairement que l'intensitÃĐ de ces raies, leur largeur, etc., informent sur les conditions physiques qui dans lesquelles se trouvent ces ÃĐlÃĐments. Les spectres en
ÃĐmission.
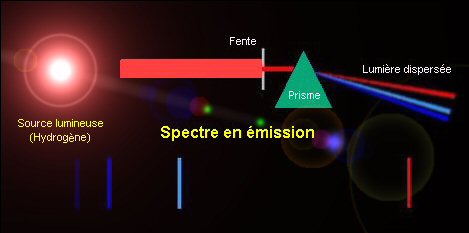 Les spectre en
absorption.
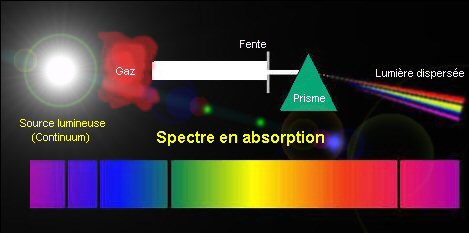 |
|||||||||||||||
Rouages |
L'origine
des raies
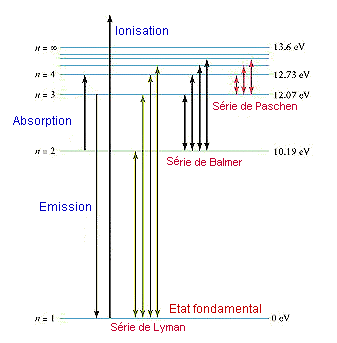
Les raies prÃĐsentes dans les spectres s'expliquent par le caractÃĻre discontinu des phÃĐnomÃĻnes physiques lorsqu'on les considÃĻre à l'ÃĐchelle microscopique, et plus spÃĐcialement à l'ÃĐchelle des atomes et des molÃĐcules. C'est le domaine de la mÃĐcanique quantique, fondÃĐe sur la notion de quantum. Un quantum correspond à la plus petite valeur que peut prendre grandeur mesurÃĐe. Toutes les autres valeurs sont des multiples de ce quantum ÃĐlÃĐmentaire. Par exemple, un quantum d'ÃĐnergie ne peut prendre que des valeurs qui sont des multiples entiers de E = hn, oÃđ h est un terme constant (constante de Planck) et n la frÃĐquence de l'onde qui transporte cette ÃĐnergie. Il s'ensuit entre autres choses de ces principes quantiques que les atomes ne peuvent stocker ou libÃĐrer de l'ÃĐnergie que sous forme discontinue. Chaque atome possÃĻde ainsi, suivant la disposition des ÃĐlectrons qu'il possÃĻde, une gamme d'ÃĐnergie qui lui sont attribuables : ce sont ses niveaux d'ÃĐnergie. Chaque niveau exprimant un ÃĐtat d'ÃĐnergie. L'ÃĐtat de plus basse ÃĐnergie que peut avoir l'enveloppe ÃĐlectronique d'un atome prend le nom d'ÃĐtat fondamental. Lorsqu'un ÃĐlectron absorbe un photon, l'ÃĐnergie globale de l'atome augmente, la configuration ÃĐlectronique change et l'atome se trouve alors dans un ÃĐtat dit excitÃĐ. Si l'ÃĐnergie absorbÃĐe est plus importante, l'ÃĐlectron peut mÊme quitter l'atome, ce qui correspond au phÃĐnomÃĻne d'ionisation. Cependant, les atomes tendent spontanÃĐment à revenir à leur ÃĐtat de plus faible ÃĐnergie (l'ÃĐtat fondamental), soit en se dÃĐbarrassant de l'ÃĐnergie emmagasinÃĐe, par sa dÃĐsexcitation (phÃĐnomÃĻne de fluorescence), soit, s'il y a eu ionisation, en rÃĐcupÃĐrant l'ÃĐlectron qui s'est ÃĐchappÃĐ (recombinaison). L'excitation,
l'ionisation ou le retour à l'ÃĐtat fondamental ne s'effectuent pas par
des chemins uniques. Les configurations ÃĐnergÃĐtiques de l'atome peuvent
correspondre transitoirement à des niveaux d'ÃĐnergie intermÃĐdiaires.
Cela conduit à l'existence à un nombre considÃĐrable (et mÊme en thÃĐorie
infini) de transitions possibles entre les diffÃĐrents ÃĐtats. Ce sont
ces transitions, qui correspondent selon les cas à des absorptions ou
à des ÃĐmissions, qui expliquent l'existence des raies spectrales.
 -
|
| . |
|
|
|
|||||||||||||||||||||||||||||||
|